2020年8月17日,中科院上海药物研究所安全评价研究中心任进研究员团队联合上海交通大学医学院附属瑞金医院研究团队分析发现了miR-552-3p可以在细胞核内发挥调控肝X受体(LXR)和法尼醇X受体(FXR)下游基因的新的生物学功能,并在多种动物模型中验证了此miRNA对肝内糖脂代谢异常的改善作用。
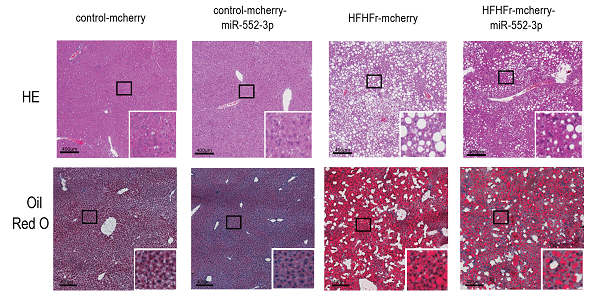
LXR和FXR属于代谢性核受体NR1家族成员,对肝内糖脂稳态调节发挥了重要作用。研究团队随后通过体外FRET、ChIP、pull down、EMSA等分子生物学技术,发现miR-552-3p序列中特有的与NR1家族响应元件类似的碱基排列,可与LXR响应元件(LXRE,DR4)序列的反义链结合,以及与FXR响应元件(FXRE,IR1)序列的正义链和反义链结合,从而影响它们的转录活性及下游糖脂代谢相关基因的表达。这一作用机制也在人的肝原代细胞上再次得到印证。此外,研究应用人的临床样本发现了miR-552-3p与NAFLD病人肝脂蓄积程度和肝损伤的相关性。
该研究首次提出了miR-552-3p对肝内糖脂代谢的调控作用,具有改善糖脂代谢紊乱的生物学功能;再次证明了本实验室首次提出的miRNA、转录因子和顺式作用元件相互作用的新分子机制;也为miR-552-3p发展成为NAFLD无创诊断的生物标志物及基于该miRNA进行糖脂代谢病的药物开发提供了可能性。如上新发现为进一步研究细胞核内miRNA调控下游基因表达提供了新机制,为miRNA参与体内糖脂代谢提供了新依据,为糖脂代谢失调性疾病的药物研发提供了新方向。
上海药物所安评中心研究团队多年致力于miRNA在疾病发生发展中的生物学功能和分子机制以及应用研究。同时也是继2016年任进研究团队在Biochimica et Biophysica Acta(BBA) gene regulatory mechanisms首次发现miR-552-3p可以同时定位于细胞核和细胞质中,通过转录和转录后双重抑制作用发挥更大的基因转录抑制作用之后,对miR-552-3p在细胞核内的生物学功能和分子机制进行的更进一步的研究。



